Cục Quản lý Dược đã ra quyết định số 483/QĐ-XPHC, xử phạt vi phạm hành chính đối với Công ty Cổ phần Dược - Trang thiết bị y tế Bình Định (Bidiphar) có địa chỉ tại số 498 đường Nguyễn Thái Học, phường Quang Trung, thành phố Quy Nhơn, tỉnh Bình Định.
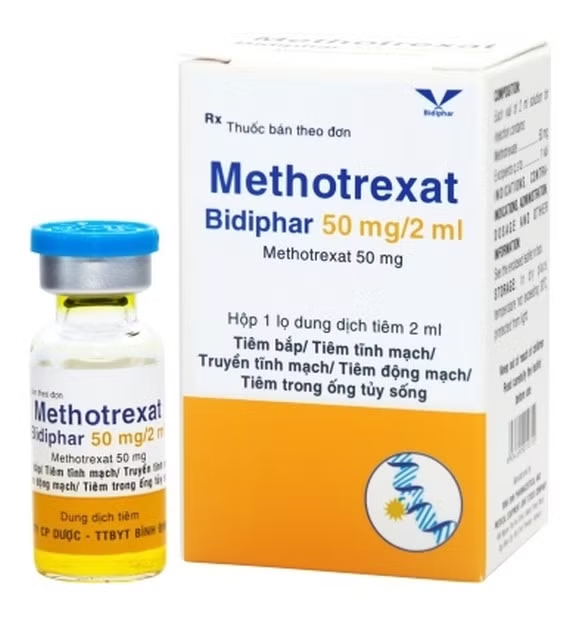
Cụ thể, Công ty cổ phần Dược - Trang thiết bị y tế Bình Định (Bidiphar) đã thực hiện hành vi vi phạm hành chính khi sản xuất thuốc vi phạm chất lượng mức độ 1 theo quy định của pháp luật đối với thuốc Methotrexat Bidiphar 50mg/2ml, số giấy đăng ký lưu hành QLĐB-638-17, số lô 21003, ngày sản xuất 30/8/2021, hạn dùng 30/8/2023.
Vi phạm quy định tại Điểm a khoản 5, điểm b khoản 8, điểm a khoản 9 Điều 57 Nghị định số 117/2020/NĐ-CP ngày 28/9/2020 của Chính phủ quy định xử phạt vi phạm hành chính trong lĩnh vực y tế (sau đây gọi tắt là Nghị định số 117/2020/NĐ-CP).
Do đó, Công ty cổ phần Dược - Trang thiết bị y tế Bình Định (Bidiphar) bị áp dụng 3 hình thức xử phạt và khắc phục hậu quả.
Thứ nhất, hành vi vi phạm quy định tại điểm a khoản 5 Điều 57 Nghị định số 117/2020/NĐ-CP: Mức phạt tiền đối với cá nhân là từ từ 40 triệu đồng đến 60 triệu đồng.
Do không có tình tiết tăng nặng, giảm nhẹ, áp dụng mức phạt tiền đối với cá nhân ở mức trung bình là 50 triệu đồng. Áp dụng quy định tại khoản 5 Điều 4 của Nghị định số 117/2020/NĐ-CP, mức phạt tiền đối với tổ chức gấp đôi mức phạt tiền đối với cá nhân là 100 triệu đồng.
Thứ hai, hình thức xử phạt bổ sung là đình chỉ hoạt động dây chuyền sản xuất liên quan đến hành vi vi phạm là dây chuyền sản xuất thuốc tiêm độc tế bào của Công ty cổ phần Dược - Trang thiết bị y tế Bình Định (Bidiphar) trong thời hạn 2 tháng kể từ ngày ban hành ban hành quyết định (ngày 7/7/2023).
Thứ ba, công ty buộc tiêu hủy toàn bộ số thuốc vi phạm chất lượng (lô thuốc Methotrexat Bidiphar 50mg/2ml, số giấy đăng ký lưu hành QLĐB-638-17, số lô 21003 ngày sản xuất 30/8/2021, hạn dùng 30/8/2023 do Công ty cổ phần Dược - Trang thiết bị y tế Bình Định (Bidiphar) sản xuất.
Đồng thời, gửi báo cáo về việc thu hồi và thực hiện biện pháp khắc phục hậu quả cho Cục Quản lý Dược trong vòng 30 ngày.
Quyết định này được giao cho bà Phạm Thị Thanh Hương, người đại diện theo pháp luật của Công ty cổ phần Dược - Trang thiết bị y tế Bình Định (Bidiphar) chấp hành. Nếu công ty không chấp hành tự nguyện trong thời hạn quy định thì sẽ bị áp dụng biện pháp cưỡng chế theo luật.
Trước đó, năm 2021, Cục Quản lý Dược - Bộ Y tế đã có thông báo thu hồi toàn quốc thuốc Methotrexat Bidiphar 50mg/2ml, số GĐKLH: QLĐB-638-17, số lô: 21003; Ngày sản xuất: 30/8/2021; Hạn sử dụng: 30/8/2023 của Công ty Cổ phần Dược - Trang thiết bị y tế Bình Định sản xuất do không đạt tiêu chuẩn chất lượng. Được biết, thuốc Methotrexat Bidiphar 50mg/2ml là thuốc điều trị cho người bệnh bạch cầu, ung thư vú, ung thư phổi, ung thư đầu và cổ.