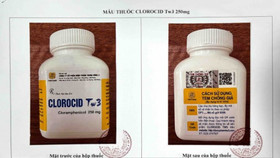
Vừa qua, các cơ quan chức năng đã phát hiện nhiều loại thuốc dạng viên nén có tên: Cefuroxim 500mg, Cefodoxim 200mg, Cefixin 200mg, Cefixim 100mg, Esomeprazol 40mg, Fluconazol 150mg.
Tất cả thuốc đều mang nhãn mác do công ty Rotexmedica GmbH, địa chỉ: Bunsenstrasse 4 - D - 22946 Trittau, sản xuất tại Germany. Nhập khẩu bởi công ty TNHH Rotex Việt Nam.

Nhưng qua rà soát, không có Công ty TNHH Rotex Việt Nam có trụ sở tại địa chỉ đăng ký kinh doanh: Ô số 22 LK 07 Khu đô thị Hùng Vương, thành phố Phúc Yên, tỉnh Vĩnh Phúc, đứng tên Đinh Ngọc Cường là đại diện công ty.
Cục Quản lý Dược khẳng định chưa cấp bất kỳ giấy đăng ký lưu hành thuốc nào cho công ty TNHH Rotex Việt Nam và chưa cấp giấy đăng ký lưu hành cho các sản phẩm thuốc dạng viên nén do công ty Rotexmedica GmbH, địa chỉ: Bunsenstrasse 4 - D - 22946 Trittau, Germany sản xuất.
Do vậy, tất cả các thuốc viên dạng viên nén trên nhãn mác công ty Rotexmedica GmbH, địa chỉ: Bunsenstrasse 4 - D - 22946 Trittau, sản xuất tại Germany và các thuốc viên nén do công ty TNHH Rotex Việt Nam nhập khẩu, phân phối trên thị trường là thuốc giả nhãn mác nhà sản xuất.
Được biết, các thuốc nói trên là dòng thuốc kháng sinh, thuốc điều trị dạ dày, thực quản, thuốc trị nấm...
Để đảm bảo an toàn cho người sử dụng, Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, Y tế địa phương thông báo cho các cơ sở kinh doanh, sử dụng thuốc không kinh doanh, phân phối và sử dụng các thuốc viên dạng nén trên nhãn mác công ty Rotexmedica GmbH, địa chỉ: Bunsenstrasse 4 - D - 22946 Trittau, Germany sản xuất và công ty TNHH Rotex Việt Nam nhập khẩu, phân phối.
Đồng thời, tăng cường việc thanh tra, kiểm tra các hoạt động kinh doanh của các cơ sở kinh doanh dược trên địa bàn, chú ý kiểm tra đối với các loại thuốc dạng viên nén nêu trên.
Ngoài ra, cần tăng cường đơn vị tiếp nhận và xác minh thông tin, báo cáo Ban chỉ đạo 389 tỉnh, thành phố và hợp tác với các cơ quan chức năng liên quan kiểm tra xác minh, truy tìm nguồn gốc xuất xứ đối với các sản phẩm thuốc giả nêu trên.
Các thông tin liên quan đến sản xuất bao gồm: số lô, ngày sản xuất, hạn dùng… có thể thay đổi do thuốc giả có thể sản xuất ghi nhãn nhiều lô khác nhau nếu phát hiện trên địa bàn.
Thêm vào đó, khẩn trương tiến hành thanh tra, kiểm tra hoạt động kinh doanh thuốc giả đối với các cơ sở kinh doanh, sử dụng thuốc nêu trên. Xử lý nghiêm các trường hợp vi phạm và gửi kết quả báo cáo kịp thời về Cục Quản lý Dược.
Cục Quản lý Dược yêu cầu các công ty sản xuất, kinh doanh, nhập khẩu, phân phối liên quan đến các sản phẩm có thông tin như mô tả nêu trên ngừng ngay việc phân phối, lưu hành thuốc giả. Thông báo cho các cơ sở kinh doanh, sử dụng đã mua thuốc dừng phân phối, sử dụng và trả về cơ sở cung ứng do công ty TNHH Rotex Việt Nam nhập khẩu.
Cung cấp thông tin và phối hợp với Sở Y tế các tỉnh, TP và các cơ quan chức năng có liên quan trong việc truy tìm nguồn gốc đối với các sản phẩm có thông tin như mô tả nêu trên.