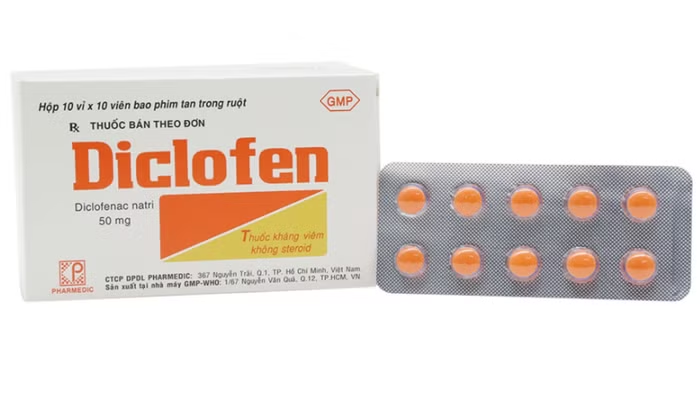
Mới đây, Cục Quản lý Dược đã ra quyết định thu hồi trên toàn quốc lô thuốc viên nén bao phim tan trong ruột Diclofen (Diclofenac natri 50mg), số giấy đăng ký lưu hành VD-25150-16, số lô 0040724, ngày sản xuất 26/7/2024, hạn dùng 26/7/2027, Công ty cổ phần dược phẩm dược liệu Pharmedic sản xuất.
Theo đó, mẫu thuốc viên nén bao phim tan trong ruột Diclofen (Diclofenac natri 50mg) nói trên được Trung tâm kiểm nghiệm thuốc, mỹ phẩm, thực phẩm TP.HCM lấy tại hộ kinh doanh nhà thuốc Phương Vy (địa chỉ 534 Nguyễn Chí Thanh, phường 7, quận 11, TP.HCM), có kết quả không đạt tiêu chuẩn chất lượng về chỉ tiêu tạp chất liên quan (vi phạm mức độ 2).
Do vậy, Công ty cổ phần dược phẩm dược liệu Pharmedic phải ngừng việc kinh doanh và tiến hành biệt trữ lô thuốc bị thu hồi còn tồn tại cơ sở. Báo cáo tình hình phân phối thuốc tới cơ sở bán buôn, cơ sở khám bệnh, chữa bệnh, gửi về Cục Quản lý Dược và Sở Y tế TP.HCM trong vòng 7 ngày kể từ ngày ban hành quyết định.
Chủ trì, phối hợp với tổ chức, cá nhân có liên quan gửi thông báo thu hồi lô thuốc bị thu hồi tới tất cả các cơ sở bán buôn, bán lẻ, cơ sở tổ chức chuỗi nhà thuốc, cơ sở khám bệnh, chữa bệnh và người sử dụng đã nhận lô thuốc nêu trên.
Tổ chức thu hồi và tiếp nhận toàn bộ lô thuốc bị thu hồi, hoàn thành trong thời hạn 15 ngày kể từ ngày ban hành quyết định này. Xử lý lô thuốc bị thu hồi, chi trả chi phí cho việc thu hồi, xử lý thuốc bị thu hồi, bồi thường thiệt hại theo quy định của pháp luật.
Việc xử lý thuốc bị thu hồi phải thực hiện theo quy định tại Điều 16, Điều 17 Thông tư số 30/2025/TT-BYT ngày 1/7/2025 của Bộ Y tế hướng dẫn áp dụng tiêu chuẩn chất lượng, kiểm nghiệm thuốc, nguyên liệu làm thuốc và thu hồi, xử lý thuốc vi phạm.
Công ty cũng cần gửi báo cáo bằng văn bản kết quả thu hồi của lô thuốc về Cục Quản lý Dược và Sở Y tế TP.HCM trong vòng 3 ngày kể từ ngày hoàn thành việc thu hồi. Báo cáo gồm các tài liệu theo quy định tại điểm a khoản 8 Điều 13 Thông tư số 30/2025/TT-BYT ngày 1/7/2025 của Bộ Y tế hướng dẫn áp dụng tiêu chuẩn chất lượng, kiểm nghiệm thuốc, nguyên liệu làm thuốc và thu hồi, xử lý thuốc vi phạm.
Cơ sở bán buôn, bán lẻ, cơ sở tổ chức chuỗi nhà thuốc phải ngừng kinh doanh, cung cấp, cấp phát lô thuốc bị thu hồi nêu trên. Đồng thời, thông báo và tổ chức thu hồi, tiếp nhận toàn bộ lô thuốc bị thu hổi, trả thuốc cho cơ sở đã cung cấp thuốc.
Cơ sở khám bệnh, chữa bệnh và người sử dụng thuốc ngừng việc kê đơn, bán, cấp phát và sử dụng lô thuốc, trả thuốc cho cơ sở cung cấp thuốc.
Sở Y tế TP.HCM kiểm tra và giám sát Công ty cổ phần dược phẩm dược liệu Pharmedic thực hiện việc thu hồi và xử lý thuốc bị thu hồi theo quy định.
Sở Y tế các tỉnh thành phố trực thuộc Trung ương, y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc về thông tin thu hồi lô thuốc không đạt chất lượng, công bố thông tin về quyết định thu hồi thuốc trên trang thông tin điện tử của Sở, kiểm tra và giám sát các đơn vị thực hiện thông báo này, xử lý những đơn vị vi phạm theo quy định hiện hành, báo cáo về Cục Quản lý Dược và các cơ quan chức năng có liên quan.
Công ty Cổ phần Dược phẩm Dược liệu Pharmedic thành lập từ năm 1981. Công ty có nhà máy sản xuất dược phẩm GMP-WHO.
Ngành nghề kinh doanh chính là sản xuất, kinh doanh dược phẩm, cung cấp những loại thuốc thiết yếu cho nhu cầu điều trị bệnh, thuốc từ dược liệu, vitamin và khoáng chất, thuốc tẩy trùng và sát khuẩn, thuốc dùng ngoài, mỹ phẩm và thực phẩm chức năng. Một số sản phẩm nổi bật của công ty gồm Bar, Gynofar, Povidine, Natri Clorid...
Diclofen là thuốc có chứa Diclofenac natri với các công dụng trị dài hạn các triệu chứng của viêm thấp khớp mãn tính (viêm đa khớp dạng thấp, viêm cứng khớp cột sống, viêm xương khớp mạn tính), thấp khớp trong bệnh vẩy nến và trị ngắn hạn các triệu chứng đau cấp tính như sau chấn thương, đau thắt lưng, đau khớp vai, cẳng tay, đau bụng do kinh nguyệt.