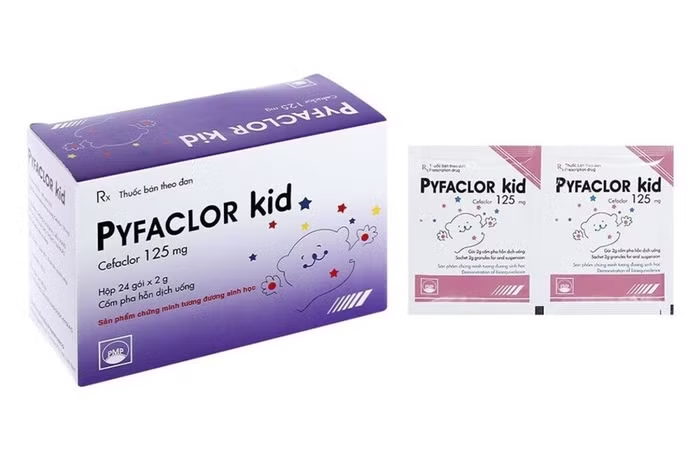
Ngày 13/10, Cục Quản lý Dược có quyết định về việc thu hồi Giấy đăng ký lưu hành thuốc tại Việt Nam đối với thuốc Pyfaclor Kid, số đăng ký VD-26427-17.
Sản phầm do Công ty Cổ phần Pymepharco (địa chỉ 166 - 170 Nguyễn Huệ, Tuy Hoà, Phú Yên) đứng tên đăng ký. Quyết định thu hồi được ban hành theo quy định tại điểm b, khoản 1, Điều 58 Luật Dược. Cụ thể, trong thời hạn 60 tháng có 2 lô thuốc bị thu hồi bắt buộc do vi phạm ở mức độ 2 hoặc 3 lô thuốc trở lên vi phạm chất lượng.
Theo quy định thu hồi thuốc của thông tư số 11/2018/TT-BYT, có 3 mức độ vi phạm chất lượng. Mức độ 1 là thuốc vi phạm có nguy cơ gây tổn hại nghiêm trọng đối với sức khỏe hoặc ảnh hưởng đến tính mạng của người sử dụng. Mức độ 2 là thuốc có bằng chứng không bảo đảm đầy đủ hiệu quả điều trị, có nguy cơ không an toàn cho người sử dụng nhưng chưa đến mức gây tổn hại nghiêm trọng đối với sức khỏe hoặc chưa ảnh hưởng đến tính mạng của người sử dụng. Mức độ 3 là thuốc không ảnh hưởng đến hiệu quả điều trị và an toàn khi sử dụng.
Loại thuốc trên không được sản xuất và lưu hành trên thị trường kể từ 13/10. Công ty Cổ phần Pymepharco phải thực hiện thu hồi thuốc nêu trên theo quy định của pháp luật.
Đồng thời, Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, các cơ sở kinh doanh dược và Giám đốc cơ sở đăng ký, sản xuất có loại thuốc trên chịu trách nhiệm thi hành quyết định này.
Trước đó, cuối tháng 9/2025, Cục Quản lý Dược đã ra quyết định về việc thu hồi trên toàn quốc lô thuốc cốm pha hỗn dịch uống Pyfaclor Kid (Cefaclor 125mg), số giấy đăng ký lưu hành VD-26427-17, số lô 410923, ngày sản xuất 13/9/2023, hạn dùng 13/9/2026.
Theo đó, xét công văn số 1086/VKNT-KHTH ngày 17/9/2025 của Viện kiểm nghiệm thuốc TP.HCM gửi kèm phiếu kiểm nghiệm số 1054/VKN-YC2025 và 1055/VKN-YC2025 ngày 17/9/2025, kết quả lấy mẫu bổ sung đối với lô thuốc cốm pha hỗn dịch uống Pyfaclor Kid nêu trên là không đạt tiêu chuẩn chất lượng về chỉ tiêu tính chất, định lượng (vi phạm mức độ 2).
Pyfaclor Kid là thuốc điều trị nhiễm khuẩn đường hô hấp trên và hô hấp dưới mức độ nhẹ và vừa, nhiễm khuẩn đường tiết niệu không biến chứng, nhiễm khuẩn da và mô mềm. Thuốc không dùng cho bệnh nhân nhạy cảm với kháng sinh nhóm cephalosporin và các thành phần khác của thuốc, trẻ em dưới 1 tháng tuổi.
Công ty cổ phần dược phẩm Pymepharco được thành lập vào năm 1989 với nhiệm vụ sản xuất dược phẩm, kinh doanh thuốc và vật tư thiết bị y tế.
Đến thời điểm này, Pymepharco đã sản xuất được nhiều dạng bào chế, đa dạng nhiều nhóm sản phẩm đáp ứng nhu cầu điều trị. Trong đó, đáng chú ý là dạng bào chế khó như viên tim mạch phóng thích hoạt chất có kiểm soát, phóng thích hoạt chất kéo dài, dạng thuốc tiêm đông khô…
Pymepharco có hơn 60 sản phẩm đã được tiến hành đánh giá tương đương sinh học tại Viện Kiểm nghiệm thuốc Trung ương và Viện Kiểm nghiệm thuốc TP.HCM, hiện tại đã có 40 sản phẩm đã được Bộ Y tế công bố.