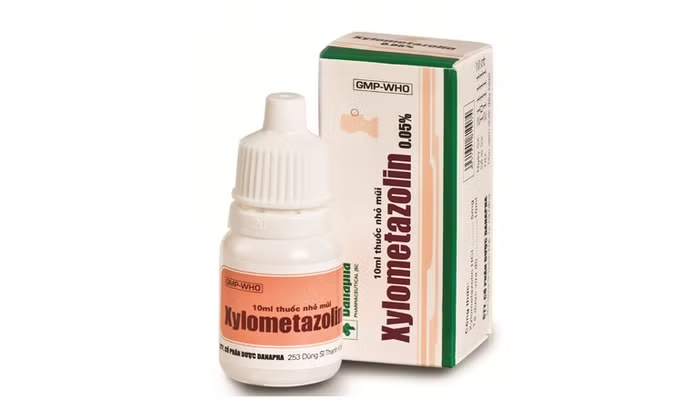
Mới đây, Cục Quản lý Dược thông báo thu hồi toàn quốc dung dịch nhỏ mũi Xylometazolin 0,05%, số lô 030523, ngày sản xuất 19/5/2023, hạn sử dụng 19/5/2025 do Công ty cổ phần dược Danapha sản xuất.
Theo đó, căn cứ công văn số 09/KN-KHTC của Trung tâm kiểm nghiệm thuốc - mỹ phẩm - thực phẩm tỉnh Hải Dương gửi kèm phiếu kiểm nghiệm, mẫu thuốc trên được xác định không đạt tiêu chuẩn chất lượng về chỉ tiêu tổng số vi sinh vật hiếu khí và trực khuẩn mủ xanh (Pseudomonas aeruginosa). Như vậy, lô thuốc nhỏ mũi được xác định là vi phạm mức độ 2.
Sau khi nhận được thông tin, Cục Quản lý Dược đã yêu cầu Công ty cổ phần dược Danapha phối hợp với nhà phân phối thuốc phải gửi thông báo thu hồi tới các cơ sở bán buôn, bán lẻ, sử dụng và tiến hành thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn chất lượng trong thời hạn 2 ngày kể từ ngày ký công văn,
Đồng thời, gửi báo cáo thu hồi về Cục Quản lý Dược trong vòng 18 ngày. Hồ sơ thu hồi bao gồm số lượng sản xuất, số lượng phân phối, ngày sản xuất, số lượng thu hồi, các bằng chứng về việc thực hiện thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng đã mua thuốc theo quy định tại thông tư số 11/2018/TT-BYT của Bộ Y tế quy định về chất lượng thuốc, nguyên liệu làm thuốc.
Bên cạnh đó, Sở Y tế các tỉnh thành phố trực thuộc trung ương, y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi lô thuốc không đạt chất lượng nêu trên.
Cùng với đó là công bố thông tin về quyết định thu hồi thuốc trên trang thông tin điện tử của Sở, kiểm tra và giám sát các đơn vị thực hiện thông báo này, xử lý những đơn vị vi phạm theo quy định hiện hành, báo cáo về Cục Quản lý Dược và các cơ quan chức năng có liên quan.
Ngoài ra, Sở Y tế tỉnh Hải Dương, Sở Y tế thành phố Đà Nẵng phải kiểm tra và giám sát Công ty cổ phần dược Danapha thực hiện việc thu hồi và xử lý thuốc bị thu hồi theo quy định.